Lecanemab ist ein Wirkstoff, der in wissenschaftlichen Studien zur Behandlung der Alzheimer-Krankheit getestet wurde. In den USA wurde der Wirkstoff am 6. Januar 2023 unter dem Handelsnamen Leqembi vorläufig zugelassen. Einige Experten sehen darin einen Wendepunkt im Kampf gegen Alzheimer, andere sind noch skeptisch.
Die schwierige Suche nach einem Heilmittel
1906 beschrieb Alois Alzheimer erstmals eine „eigentümliche Krankheit“, die durch schweren Gedächtnisverlust und Veränderungen der Gehirnstruktur gekennzeichnet ist. 1995 wurden seine handschriftlichen Aufzeichnungen über die 51-jährige Patientin Auguste Deter wiederentdeckt. Daraus geht hervor, dass sie bis März 1901 gesund schien. Doch dann begann mit einem paranoiden Anfall ein rapider geistiger Verfall.
Die Patientin verlor die zeitliche und räumliche Orientierung. Als sie schließlich versucht zu schreiben, wiederholt sie immer wieder denselben Satz: „Ich habe mich verloren“.
Die Worte von Auguste Deter werden vielen der Millionen Betroffenen und ihren Pflegern bekannt vorkommen. Die Alzheimer-Krankheit ist durch Gedächtnisverlust, Verwirrtheit, Persönlichkeitsveränderungen und Verlust der Unabhängigkeit gekennzeichnet. Obwohl die Krankheit seit mehr als einem Jahrhundert bekannt ist, hat es bisher kaum Fortschritte in der Behandlung gegeben.
Lecanemab: Wendepunkt im Kampf gegen Demenz?
In Deutschland sind schätzungsweise mindestens 1,8 Millionen Menschen an Demenz erkrankt, zwei Drittel davon an Alzheimer. Mit zunehmender Alterung der Bevölkerung wird die Zahl der Demenzkranken weiter ansteigen, was die Probleme noch verstärken wird.
Kein Wunder also, dass die Meldungen über den Durchbruch des Medikaments Lecanemab so viel Aufsehen erregt haben. Eine Studie legt nahe, dass Lecanemab die mit der Alzheimer-Krankheit verbundenen Gehirnveränderungen rückgängig machen und den geistigen Verfall verlangsamen kann. Die Nachricht wurde von einigen Forschern und Patientengruppen mit Begeisterung aufgenommen.
Die Ergebnisse einer Phase-III-Studie mit Lecanemab wurden am 29. November 2022 auf einer Konferenz in San Francisco vorgestellt und gleichzeitig im renommierten New England Journal of Medicine veröffentlicht.
Sie zeigten, dass Lecanemab-Infusionen in einer 18-monatigen Studie mit fast 1.800 Teilnehmern mit leichter bis mittelschwerer Erkrankung den kognitiven Verfall im Vergleich zu einer Placebo-Behandlung um 27 Prozent verlangsamten – wenn auch nicht umkehrten. Scans zeigen, dass die Antikörpertherapie die krankheitsbedingten Plaques im Gehirn wirksam beseitigt.
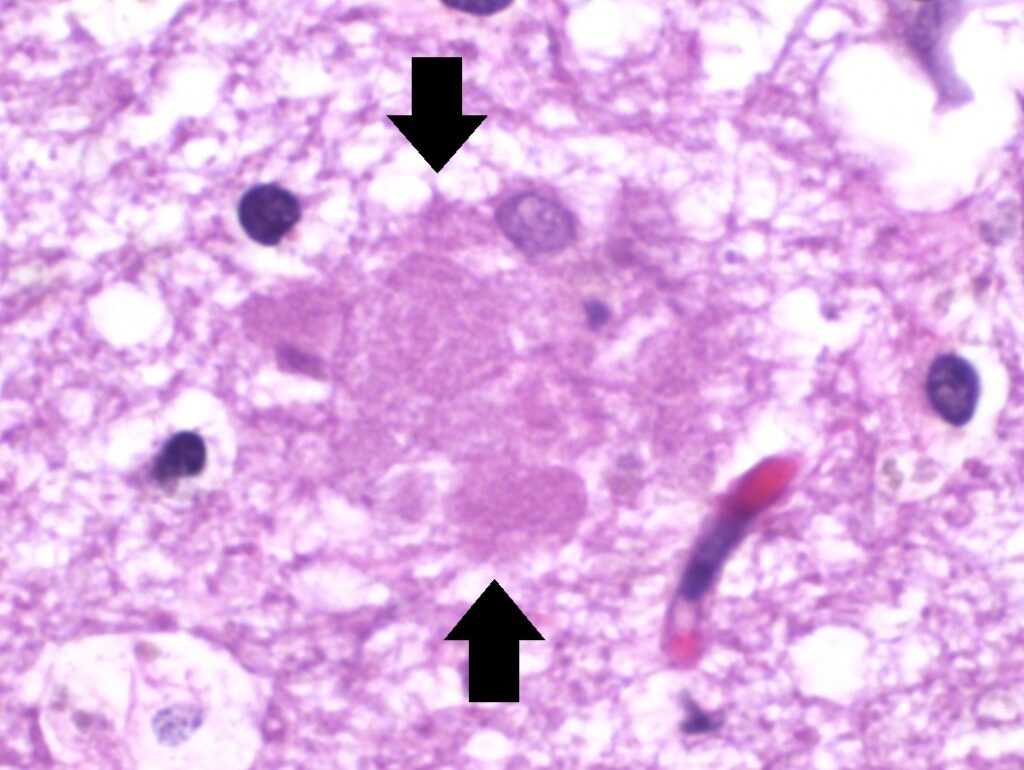
Histopathologie der Amyloid-Plaques im Hippocampus bei der Alzheimer-Krankheit.
Uneinigkeit unter Experten
Prof. Frank Jessen, Gruppenleiter am Deutschen Zentrum für Neurodegenerative Erkrankungen (DZNE) und Direktor der Klinik und Poliklinik für Psychiatrie und Psychotherapie der Universität zu Köln, begrüßt die Nachricht: „Für uns Kliniker, die mit Alzheimer-Patienten arbeiten, ist das Ergebnis der Studie ein Durchbruch. Mit diesem Antikörper hätten wir bei der Suche nach wirksamen Therapien gegen Alzheimer erstmals einen Wirkstoff in der Hand, mit dem wir wirklich kausal in den Krankheitsprozess eingreifen könnten“.
Der renommierte Hirnforscher Prof. Christian Haass, Gruppenleiter und Standortsprecher des DZNE, bezeichnete die Ergebnisse als vielversprechend. „Der Ansatz, Alzheimer mit Antikörpern zu behandeln, ist nicht gescheitert, wie in den vergangenen Jahren oft prophezeit wurde“, sagte er in einem Interview.
Der Ansatz, Alzheimer über Antikörper zu behandeln, ist nicht gescheitert, wie es in den vergangenen Jahren oft prophezeit wurde.
Experten wie Jessen und Haass sehen in den Lecanemab-Ergebnissen eine Bestätigung für eine Theorie, die zwar nicht unumstritten ist, aber die Alzheimer-Forschung beherrscht: die Amyloid-Hypothese. Sie besagt, dass bei Alzheimer-Patienten große Ansammlungen des Proteins Beta-Amyloid im Gehirn zum Absterben von Nervenzellen und zu Hirnschäden führen.
Zufälligerweise hatte kurz vor der Veröffentlichung dieser Ergebnisse der Neurobiologe Karl Herrup ein Buch über die leidvolle Geschichte der Alzheimer-Krankheit mit dem Titel How Not to Study a Disease veröffentlicht. Darin stellt Herrup mit einer gewissen Ironie fest, dass nach der Veröffentlichung eines einflussreichen Artikels von John Hardy und Gerald Higgins über die Amyloid-Hypothese im Jahr 1992 viele im medizinischen Establishment zu dem Schluss kamen, dass Alzheimer-Forscher, die sich nicht mit Amyloid beschäftigten, die Krankheit eigentlich gar nicht untersuchten.
Vorsichtiger Optimismus
In unruhigen Zeiten stürzen sich die Medien gerne auf gute Nachrichten. So auch in diesem Fall. Einige Experten sind jedoch skeptischer. Zu ihnen gehört der Neurologe Prof. Richard Dodel, Ärztlicher Direktor des Geriatriezentrums Haus Berge in Essen. „Wenn eine Studie groß genug ist, sind auch kleine Unterschiede statistisch signifikant, aber ist der Effekt auch für den einzelnen Patienten spürbar?“ Er weist vor allem darauf hin, dass die in der Studie berichteten Vorteile äußerst gering waren.
Technisch gesehen brachte Lecanemab den Patienten nur einen kleinen Vorteil von 1,4 Punkten auf der ADAS-cog14-Skala (eine 90-Punkte-Skala zur Messung von Gedächtnis, Aufmerksamkeit und Sprachfähigkeit). Für einen signifikanten Nutzen sind das Peanuts. „Der Patient merkt davon kaum etwas“, gibt auch Prof. Stefan Teipel vom DZNE zu bedenken.

Auguste Deter aus Kassel war die erste Person, bei der die Alzheimer-Krankheit diagnostiziert wurde.
Bei der Vorstellung der Ergebnisse in San Francisco präsentierten die Forscher eindrucksvolle Diagramme – Extrapolationen – die zeigten, wie sich diese bescheidenen Vorteile im Laufe der Zeit in zusätzliche Monate mit besserer Lebensqualität für die Patienten verwandeln würden. Rob Howard, Professor für Gerontopsychiatrie am University College London, der die Präsentation der Ergebnisse der Lecanemeb-Studie verfolgte, gab jedoch zu bedenken: „Wir können diese Annahmen nicht machen, weil wir wissen, dass der Krankheitsverlauf in der Regel nicht linear ist.
Eine weitere Frage ist die Sicherheit. Berichte über zwei Todesfälle durch Schlaganfall, die von einigen Forschern auf eine Nebenwirkung des Medikaments zurückgeführt werden, geben Anlass zur Sorge – insbesondere bei Patienten, die nicht sehr krank waren. Bei etwa 20 % der mit Lecanemab behandelten Patienten zeigten sich in den Hirnscans Auffälligkeiten, die auf Schwellungen oder Blutungen hindeuteten – obwohl nur eine Minderheit Symptome zeigte, die mit diesen Veränderungen in Zusammenhang standen.
Ein anderer Skeptiker ist Professor George Perry, Neurobiologe an der Universität von Texas in San Antonio, der sich mit den biochemischen Ursachen des Zelltods bei Alzheimer beschäftigt. „Warum sprechen wir von einem Durchbruch? Ich halte die Studie aus drei Gründen nicht für eine gute Nachricht“, sagt er. „Erstens sind zwei Patienten gestorben. Eine von ihnen war offenbar zwei Tage vor ihrem Tod segeln. Sie war nicht besonders krank. Zweitens waren die berichteten Vorteile nicht besser als die von Aricept (auch bekannt als Donepezil, ein älterer Acetylcholinesterase-Hemmer). „Drittens basiert all dies immer noch auf der unbewiesenen Vorstellung, dass Amyloid die Krankheit verursacht.“ Er glaubt, dass die Dominanz dieser Theorie eine gefährliche Ablenkung gewesen sein könnte.
Die Amyloid-Hypothese ist nicht unumstritten
Mehrere Faktoren werden mit der Zerstörung von Nervenzellen in Verbindung gebracht, die zu den Symptomen der Alzheimer-Krankheit führt. Ein Hauptmerkmal der Krankheit ist die Anhäufung eines Proteins namens Tau im Gehirn, das in den Nervenzellen verklumpt und deren Kommunikationsfähigkeit beeinträchtigt.
Es ist bekannt, dass auch die Gene eine Rolle spielen, denn ein kleiner Teil der Alzheimer-Fälle – etwa 5 Prozent – tritt aufgrund spezifischer Gendefekte bereits in jungen Jahren auf. Auch Infektionen können das Demenzrisiko erhöhen. Ein Teil der Forschung konzentriert sich beispielsweise auf die Rolle von Bakterien, die Zahnfleischerkrankungen verursachen.
Einige Studien haben einen Zusammenhang zwischen der Alzheimer-Krankheit und Schlafstörungen festgestellt. Kürzlich wurde entdeckt, dass schädliche Proteine während des Schlafs durch das glymphatische System, das Abfallbeseitigungssystem des Gehirns, entfernt werden.
Viele Forscher gehen daher davon aus, dass Amyloid nicht der einzige Faktor oder gar die Hauptursache der Krankheit ist.
Lecanemab: im Vergleich sehr teuer
Tatsächlich könnten ältere Medikamente wie Donepezil, die den Patienten eine bescheidene Linderung ihrer Symptome verschaffen, indem sie die Konzentration der Nervenbotenstoffe im Gehirn erhöhen, doppelt so wirksam sein wie Lecanemab – und das zu geringeren Kosten, da sie inzwischen als Generika erhältlich sind. Die gemeinsamen Entwickler von Lecanemab, Eisai und Biogen, erklärten gegenüber dem Magazin Forbes, dass die Kosten für die Hightech-Antikörpertherapie zwischen 9.000 $ (8.439 €) und 35.000 $ (32.792 €) pro Jahr und Person liegen könnten, sofern sie zugelassen wird.
Die Ereignisse ähneln stark denen, die vor etwa anderthalb Jahren bei einem anderen Alzheimer-Medikament zu beobachten waren. Im Juni 2021 genehmigte die US-amerikanische Food and Drug Administration (FDA) den Antikörper Aducanumab von Biogen mit der Begründung, dass er Amyloid aus den Gehirnen der Patienten entferne. Biogen konnte auch damals keinen signifikanten klinischen Nutzen oder gar eine statistisch signifikante Verkürzung des Krankheitsverlaufs nachweisen.
Wichtig: frühzeitige Behandlung
Die Amyloid-Hypothese hat starke Befürworter. Einer von ihnen ist Prof. Rudolf Tanzi, Neurologe an der Harvard Medical School. Er entdeckte eine Reihe von Genen, die mit der familiären Frühform der Alzheimer-Krankheit in Verbindung stehen. Defekte Gene führen dazu, dass die Betroffenen früh im Leben große Mengen Amyloid bilden und mit Mitte 50 sterben. Für Tanzi zeigt dies, dass Amyloid ein Schlüsselfaktor bei der Krankheitsentstehung ist.
Vereinfacht ausgedrückt vermutet er, dass große Mengen des Eiweißes Amyloid schließlich Plaques zwischen den Nervenzellen bilden. Diese lösen die Verklumpung des Tau-Proteins aus, das sich häufig in den Gehirnzellen der Patienten findet. Diese Verklumpungen, so Tanzi, sind es, die die körpereigenen Immunzellen dazu veranlassen, mit der Zerstörung von Hirngewebe zu beginnen.
Tanzi glaubt, dass es, wenn die Mikrogliazellen ihre Zerstörungsorgie beginnen, zu spät sein könnte, um den Schaden durch Entfernung der Amyloid-Plaques zu behandeln oder rückgängig zu machen. Er ist überzeugt, dass eine frühzeitige Behandlung – Jahrzehnte vor dem Auftreten von Symptomen – mit Amyloid abbauenden Medikamenten die Lösung ist. „Wenn man morgen alle Amerikaner testen würde, würden 40 Millionen ihren Arzt anrufen und nach einer Immuntherapie fragen“, sagt er. Er vergleicht hohe Amyloidwerte mit hohen Cholesterinwerten, die frühzeitig behandelt werden müssen. „Es geht darum, den Patienten frühzeitig sichere und kostengünstige Medikamente zur Verfügung zu stellen“, sagt er.
Es bleibt jedoch die schwierige Frage, wie man so viele Menschen testen und mit welchen Medikamenten man sie behandeln kann. Martin Rossor, Professor für klinische Neurologie am Institut für Neurologie am UCL, stimmt zu, dass die Verarbeitung von Amyloid bei der familiären Alzheimer-Krankheit im Frühstadium eine Schlüsselrolle spielt. Es ist jedoch unklar, inwieweit sich diese Rolle auf andere Formen der Alzheimer-Krankheit übertragen lässt.
War Lecanemab erst der Anfang?
Martin Rossor geht davon aus, dass es in den nächsten Jahren nicht nur neue Medikamente geben wird, die Amyloid beseitigen. Er hofft auch auf Medikamente, die auf Tau abzielen, sowie auf Therapien, die die Immunreaktion im Gehirn verändern.
Bis zum Durchbruch der pharmazeutischen Forschung gibt es aber noch andere Probleme zu lösen. Der Fachkräftemangel im Gesundheitssystem führt dazu, dass viele Patienten monatelang auf einen Spezialisten und einen Hirnscan warten. Wenn die Politik nichts unternimmt, wird sich die Lage weiter verschlechtern. Irgendwann könnte die Situation eintreten, dass Menschen auf Wartelisten so lange warten müssen, bis ihre Krankheit zu weit fortgeschritten ist, um ein möglicherweise lebensveränderndes Medikament zu erhalten. Bei Menschen mit fortgeschrittener Krankheit können auch die neuen Antikörper nichts mehr ausrichten. Der gesellschaftliche, politische und wissenschaftliche Kampf gegen die Alzheimer-Krankheit hat also gerade erst begonnen.
Quelle: inews.co.uk
 AChE-Hemmervor 3 Jahren
AChE-Hemmervor 3 Jahren
 Antidementivavor 5 Jahren
Antidementivavor 5 Jahren
 Antidementivavor 5 Jahren
Antidementivavor 5 Jahren
 Antidepressivavor 4 Jahren
Antidepressivavor 4 Jahren
 Antidepressivavor 4 Jahren
Antidepressivavor 4 Jahren
 Antidementivavor 5 Jahren
Antidementivavor 5 Jahren
 Antidepressivavor 5 Jahren
Antidepressivavor 5 Jahren
 Antidementivavor 6 Jahren
Antidementivavor 6 Jahren







Pingback: Lecanemab: ein neues Alzheimer-Medikament – Aricept
Pingback: Auf der Suche nach einem Impfstoff gegen Alzheimer - demenz-medikamente.com
Pingback: Welche Alzheimer-Medikamente gibt es?